
Wieloośrodkowa ocena kontynuacji i bezpieczeństwa leczenia tofacytynibem w RZS
Celem wieloośrodkowego, retrospektywnego badania kohortowego prowadzonego w warunkach praktyki klinicznej była ocena skuteczności i bezpieczeństwa stosowania tofacytynibu (TOFA) w leczeniu reumatoidalnego zapalenia stawów. Lek ten może stanowić cenną opcję terapeutyczną u pacjentów z RZS w połączeniu z personalizowaną kontrolą ryzyka CV.
Autorzy: Anna Felis-Giemza1, Mateusz Moskal2, Krzysztof Proc3, Zbigniew Guzera4, Marcin Stajszczyk5, Karolina Palej1, Kornelia Chmurzyńska6, Piotr Wiland7, Krzysztof Batko8, Bogdan Batko2
1Centrum Terapii
Biologicznej, Narodowy Instytut Geriatrii, Reumatologii i Rehabilitacji w Warszawie
2Katedra Reumatologii i Immunologii, Wydział
Lekarski i Nauk o Zdrowiu, Uniwersytet im. Andrzeja Frycza
Modrzewskiego w Krakowie
3Oddział Kliniczny Reumatologii
i Chorób Wewnętrznych, Uniwersytecki Szpital Kliniczny we Wrocławiu
4Świętokrzyskie Centrum Reumatologii, Szpital św.
Łukasza w Końskich
5Klinika Reumatologii i Chorób
Autoimmunologicznych, Śląskie Centrum Reumatologii, Ortopedii
i Rehabilitacji w Ustroniu
6Klinika Chorób Tkanki Łącznej,
Narodowy Instytut Geriatrii, Reumatologii i Rehabilitacji w Warszawie
7Klinika Reumatologii i Chorób Wewnętrznych, Uniwersytet
Medyczny we Wrocławiu
8Dział Badań i Rozwoju,
Fundacja Towarzystwa Prawa Gospodarki Medycznej (MELS) w Krakowie
Wieloośrodkowa ocena kontynuacji i bezpieczeństwa leczenia tofacytynibem w reumatoidalnym zapaleniu stawów – dlaczego czynniki ryzyka sercowo-naczyniowego nie są równoznaczne z ryzykiem jawnym
Streszczenie
Wprowadzenie: Celem wieloośrodkowego,
retrospektywnego badania kohortowego prowadzonego w warunkach praktyki
klinicznej była ocena skuteczności i bezpieczeństwa stosowania
tofacytynibu (TOFA) w leczeniu reumatoidalnego zapalenia stawów (RZS).
Materiał i metody: Do badania włączono 209
pacjentów z czynną postacią RZS leczonych TOFA i niereagujących na co
najmniej dwa konwencjonalne syntetyczne leki modyfikujące przebieg choroby.
Charakterystykę kliniczną uzyskano z dokumentacji elektronicznej,
uzupełniono ręcznym przeglądem dokumentacji medycznej i połączono
z danymi dotyczącymi opieki ambulatoryjnej. Oceniono wskaźnik kontynuacji
stosowania leku oraz przyczyny jego odstawienia.
Wyniki: Mediana (zakres międzykwartylowy)
czasu obserwacji w całej próbie wyniosła 16,9 (5,93–31,7) miesiąca. Średni
wiek (odchylenie standardowe) wynosił 51,44 ±11,84 roku, przeważały kobiety (n
= 168; 80,4%). Tylko u 30 pacjentów (14,4%) w momencie rozpoczęcia
leczenia TOFA nie występował żaden tradycyjny czynnik ryzyka
sercowo-naczyniowego (cardiovascular – CV). Wskaźniki kontynuacji
leczenia TOFA były wysokie, a medianę przeżycia oszacowano na 89,3% po 6
miesiącach, 82,4% po 12 miesiącach i 60,4% po 24 miesiącach. Główną
przyczyną przerwania leczenia była nieskuteczność (n = 50). Częstość
występowania zdarzeń niepożądanych była stosunkowo niska, a najczęstszymi
były zaburzenia lipidowe, zmiany w morfologii krwi i infekcje. Nie
zgłoszono żadnych poważnych zdarzeń niepożądanych dotyczących układu CV.
Częstość występowania zdarzeń niepożądanych wymagających zmiany leczenia
wyniosła 60,34 (95% CI: 37–92) na 1000 osobolat obserwacji. Obecność wielu
(>3) czynników ryzyka CV była związana z niższym prawdopodobieństwem
kontynuacji leczenia TOFA i mniejszą skutecznością leczenia.
Wnioski: Tofacytynib
charakteryzował się wysokim wskaźnikiem kontynuacji leczenia i korzystnym
profilem bezpieczeństwa u pacjentów z RZS, w tym
u pacjentów z tradycyjnymi czynnikami ryzyka CV. Lek ten może
stanowić cenną opcję terapeutyczną u pacjentów z RZS
w połączeniu z personalizowaną kontrolą ryzyka CV. Uzasadnione są
dalsze badania w celu ustalenia długoterminowych efektów stosowania TOFA
i jego wpływu na CV w większych populacjach.
Wprowadzenie
Inhibitory kinaz janusowych (Janus kinase inhibitors – JAKi) to innowacyjne, doustne, celowane syntetyczne leki przeciwreumatyczne modyfikujące przebieg choroby (csLMPCh), które zmieniły krajobraz terapeutyczny w chorobach autoimmunologicznych i zapalnych, w tym w chorobach reumatycznych układu mięśniowo-szkieletowego (rheumatic musculoskeletal diseases – RMD). Wraz z ciągłym rozwojem leków zarówno selektywne, jak i nieselektywne JAKi pojawiły się jako opcje terapeutyczne w przypadku takich chorób, jak reumatoidalne zapalenie stawów (RZS), łuszczycowe zapalenie stawów (ŁZS) i zesztywniające zapalenie stawów kręgosłupa (ZZSK) (tab. I).


Złagodzenie objawów chorobowych dotyczących stawów, skóry i jelit sprawiło, że JAKi stały się skuteczną formą terapii RMD. Ze względu na dłuższą obecność na rynku profil bezpieczeństwa JAKi opisywano jako podobny do innych leków biologicznych, chociaż nadal istnieją obawy dotyczące nadmiernego ryzyka wystąpienia niektórych zdarzeń niepożądanych [ZN: zakażenia wirusem półpaśca (HZV), chorób sercowo-naczyniowych (cardiovascular – CV) i nowotworów złośliwych] [1].
W 2012 r. amerykańska Agencja ds. Żywności i Leków (Food and Drug Administration – FDA) po raz pierwszy zarejestrowała tofacytynib (TOFA) do stosowania w leczeniu RZS. W kolejnych latach wskazania do stosowania TOFA rozszerzono o leczenie ŁZS, młodzieńczego idiopatycznego zapalenia stawów (MIZS), ZZSK i wrzodziejącego zapalenia jelita grubego (WZJG) [1, 2].
Ze względu na zgłaszane zaburzenia lipidowe producent leku zobowiązał się do wdrożenia strategii oceny i łagodzenia ryzyka. Zaprojektowano duże badanie w celu oceny ryzyka wystąpienia chorób CV i nowotworów złośliwych u pacjentów z RZS leczonych TOFA. Porównano dwie dawki (5 mg i 10 mg dwa razy na dobę) ze stosowaniem inhibitora czynnika martwicy nowotworu (tumor necrosis factor inhibitor – TNFi) u pacjentów w wieku powyżej 50 lat, z niewystarczającą odpowiedzią na metotreksat (MTX) i co najmniej jednym współistniejącym czynnikiem ryzyka CV na wizycie początkowej. Wszyscy uczestnicy otrzymywali terapię skojarzoną w postaci TOFA i MTX [3].
W 2019 r. wstępne badanie wykazało podwyższone, zależne od dawki ryzyko zatorowości płuc we wszystkich grupach wiekowych oraz zwiększoną umieralność wśród pacjentów powyżej 65. roku życia, co doprowadziło do zmniejszenia dawki u osób przyjmujących TOFA w dawce 10 mg [3].
Europejska Agencja Leków (European Medicine Agency – EMA) ograniczyła stosowanie TOFA we wszystkich wskazaniach u pacjentów powyżej 65. roku życia, podkreślając konieczność zachowania ostrożności i uzależniając jego stosowanie od możliwości przyjęcia alternatywnych schematów leczenia [4]. Amerykańska Agencja ds. Żywności i Leków zaleciła unikanie stosowania TOFA u pacjentów z podwyższonym ryzykiem rozwoju zakrzepicy naczyń. Ponadto, ponieważ dawkę 10 mg stosowano wyłącznie w badaniach z udziałem pacjentów z WZJG, jej zastosowanie w tym wskazaniu ograniczono do przypadków niewystarczającej odpowiedzi lub nietolerancji TNFi [5].
Badanie ORAL Surveillance [3] dostarczyło kilku ważnych informacji. Analiza główna sugeruje podwyższone ryzyko zgonu, poważnych niepożądanych zdarzeń sercowo-naczyniowych (major adverse cardiovascular events – MACE), nowotworów złośliwych i infekcji w obu grupach TOFA, niezależnie od schematu dawkowania, w porównaniu z TNFi. Warto zauważyć, że parametry skuteczności były porównywalne między uczestnikami stosującymi TOFA i TNFi [3]. Następnie FDA ograniczyła stosowanie wszystkich JAKi w leczeniu RMD, uzasadniając tę decyzję możliwością wystąpienia efektu klasy, co wymaga zachowania szczególnej ostrożności (tab. I) [6].
W regionie europejskim EMA rozszerzyła podobne zalecenia na inne JAKi (w tym filgotynib, który nie jest zarejestrowany przez FDA), choć przepisy są mniej restrykcyjne i dopuszczają możliwość modyfikacji dawki w ramach strategii ograniczania ryzyka (tab. I) [7].
Pilnie potrzebne są dane z praktyki klinicznej z różnych regionów geograficznych, aby pomóc klinicystom i decydentom w optymalizacji kontrolowania RMD i regulacji prawnych. Nasza wiedza na temat profilu bezpieczeństwa JAKi jest nadal częściowa, a analizy post hoc dotyczące raportu z badania ORAL Surveillance podkreślają znaczenie jawnej choroby CV na wizycie początkowej [8, 9].
Według niektórych doniesień u 78,5% chorych na RZS można zaobserwować co najmniej jeden modyfikowalny czynnik ryzyka CV [10]. Różnice dotyczące prognostycznego znaczenia tradycyjnych czynników ryzyka CV w porównaniu z istnieniem zdarzeń CV w wywiadzie również pozostają niejasne. Z perspektywy pacjenta podwyższone ryzyko CV zalicza się do najmniej akceptowalnych ZN w terapii RZS [11]. Dlatego zgłaszanie danych z badań obserwacyjnych, w których analizowane są te czynniki, może mieć kluczowe znaczenie dla przyszłych inicjatyw, które pozwolą ocenić, połączyć oraz ilościowo określić ryzyko związane ze stosowaniem JAKi.
Celem tego retrospektywnego badania jest ocena poziomu kontynuacji leczenia i bezpieczeństwa TOFA na podstawie wieloośrodkowej kohorty pacjentów z RZS. Czynniki ryzyka oceniano w momencie rozpoczęcia leczenia oraz prowadzono sekwencyjną obserwację w celu oceny skuteczności leku (przy użyciu złożonych parametrów) i profilu bezpieczeństwa.
Materiał i metody
Retrospektywne badanie kohortowe zaprojektowano w celu oceny bezpieczeństwa i skuteczności TOFA w leczeniu RZS w praktyce klinicznej. W badaniu wzięło udział pięć specjalizujących się w dziedzinie reumatologii ośrodków trzeciego stopnia referencyjności z różnych regionów Polski.
W okresie od czerwca do sierpnia 2023 r. autorzy korzystali z metody dogodnego doboru próbek i rekrutowali pacjentów na podstawie elektronicznej dokumentacji medycznej uzyskanej z obowiązkowego rejestru innowacyjnych terapii, uzupełnionej ręcznym przeglądem dokumentacji medycznej (wykonywanym przez specjalistów lub stażystów z zakresu reumatologii). Korzystając z powiązań z lokalnymi przychodniami, uzupełniono także dane dotyczące skuteczności i bezpieczeństwa. Pacjenci rozpoczynali stosowanie TOFA po niepowodzeniu co najmniej dwóch konwencjonalnych terapii LMPCh.
Kryteria włączenia zostały określone a priori w następujący sposób: (1) wiek powyżej 18 lat, (2) potwierdzone rozpoznanie RZS zgodnie z kryteriami klasyfikacji EULAR (European Alliance of Associations for Rheumatology) i Amerykańskiego Kolegium Reumatologicznego (American College of Rheumatology – ACR), (3) jakiekolwiek użycie TOFA (w dowolnej dawce) w okresie od lipca 2018 r. do września 2023 r. Z udziału wykluczono pacjentów z jawną chorobą CV.
Ostateczny zbiór danych zawierał informacje na temat cech demograficznych, rozpoznania zapalenia stawów, pomiarów antropometrycznych, schematów leczenia, obecności czynników ryzyka CV na wizycie początkowej oraz szczegółowe informacje na temat ZN, a także złożone parametry aktywności choroby. Kontrolę sekwencyjną ustalono na podstawie zapisów wizyt zarejestrowanych w ustalonym horyzoncie czasowym obserwacji, zgodnie z programem lekowym, który umożliwia finansowanie innowacyjnych metod leczenia w Polsce. Dane uzyskano dla miesięcy 0, 3. i 6. oraz ostatniej dostępnej wizyty (do września 2023 r.).
W stosownych przypadkach zarejestrowano dostępne informacje opisowe w celu dalszej oceny przyczyn przerwania leczenia.
Określono ryzyko CV, stosując tradycyjne definicje czynników ryzyka: palenie tytoniu (zdefiniowane jako zmienna porządkowa; palenie tytoniu obecnie, kiedykolwiek i nigdy), wiek (50 lat i więcej), nadciśnienie tętnicze, cukrzyca, udokumentowana historia zdarzeń CV, dyslipidemia, wskaźnik masy ciała (body mass index – BMI) powyżej 25 kg/m2. Czynniki ryzyka nie obejmowały dawki glikokortykosteroidów (GKS), a informację o ostatniej dostępnej dawce traktowano jako uzupełniającą, ponieważ nie można było wiarygodnie obliczyć skumulowanej dawki GKS. Zaprzestanie terapii sklasyfikowano na podstawie uzasadnienia klinicznego: niewystarczająca odpowiedź na leczenie, wystąpienie ZN i inne przyczyny.
Dane zanonimizowano przed analizą. Przeanalizowano całą dokumentację chorych rozpoczynających leczenie TOFA, dla których dostępna była odpowiednia data rozpoczęcia leczenia i w przypadku których można było wiarygodnie wyodrębnić informacje uzupełniające (wizyty rejestrowane przez co najmniej 0, 3 i 6 miesięcy). Pacjentów określano jako: survivors (osoby, które kontynuowały leczenie TOFA do ostatniej zarejestrowanej wizyty), osoby zmieniające leczenie (u których leczenie zostało zmodyfikowane z dowolnej przyczyny), osoby z odpowiedzią i osoby bez odpowiedzi na leczenie (odpowiednio: wystarczająca lub niewystarczająca odpowiedź na terapię zgodnie z wytycznymi programu leczenia).
Pierwszorzędowe wyniki badania zdefiniowano
w następujący sposób:
● kontynuacja leczenia TOFA po 6 miesiącach w całej próbie,
● przeżycie wolne od ZN wymagających zmiany leku
wśród osób z odpowiedzią na leczenie po 6 miesiącach.
Drugorzędowe punkty końcowe obejmowały:
● kontynuację leczenia i przeżycie wolne od ZN (lub nieskuteczności) po
12 i 24 miesiącach,
● częstość występowania ZN o szczególnym znaczeniu na 1000 pacjentolat:
MACE, żylna choroba zakrzepowo-zatorowa (ŻChZZ) lub nowotwór złośliwy,
● przewidywane prawdopodobieństwo nieskuteczności leku, wpływ ryzyka CV na
kontynuację leczenia i występowanie ZN.
Analiza statystyczna
Analizę statystyczną przeprowadzono za pomocą oprogramowania R 4.3.2 (R Core Team, 2023, R Foundation for Statistical Computing, Wiedeń, Austria). Zmienne ciągłe i dyskretne podsumowano, odpowiednio, za pomocą średniej z odchyleniem standardowym (SD) lub liczby i odsetka (n, %). Brakujące dane przypisano przy użyciu wartości modalnych i median, odpowiednio dla zmiennych nominalnych i ciągłych.
Rozkład zmiennej sprawdzano wizualnie za pomocą wykresów gęstości oraz przeprowadzano odpowiednią transformację w przypadku, gdy rozkład był skośny. Porównanie między grupami przeprowadzono za pomocą testu t i testu dokładnego Fishera, odpowiednio dla zmiennych ciągłych i nominalnych.
Przeżycie oceniano za pomocą surowych krzywych Kaplana-Meiera oraz modeli hazardów proporcjonalnych Coxa (PH), przy czym założenie dotyczące PH sprawdzano przy użyciu reszt Schoenfelda. Testy były dwustronne, a wartość p poniżej 0,05 uznawano za istotną.
Standardy bioetyczne
Badanie było zgodne ze standardami etycznymi według Deklaracji Helsińskiej oraz krajowymi przepisami w tej dziedzinie. Zgoda komisji bioetycznej nie była wymagana, ponieważ było to nieinterwencyjne, retrospektywne badanie bazy danych oparte na danych zebranych w trakcie leczenia. Rutynowo, zgodnie z ustalonymi zasadami, wszyscy pacjenci byli informowani o metodzie leczenia i działaniu leku, a następnie wyrażali świadomą zgodę na leczenie. Wszystkie ośrodki otrzymały uprawnienia administracyjne do przetwarzania danych.
Wyniki
Do udziału w badaniu zakwalifikowano ogółem 223 pacjentów z RZS, z czego wykluczono 14 pacjentów (12 ze względu na historię zdarzeń CV i 2 z powodu brakujących danych). Ostateczna próba obejmowała 209 pacjentów z RZS. Średni wiek (SD) dla tej próby wynosił 51,44 ±11,84 roku, a większość stanowiły kobiety (168; 80,4%) (tab. II).
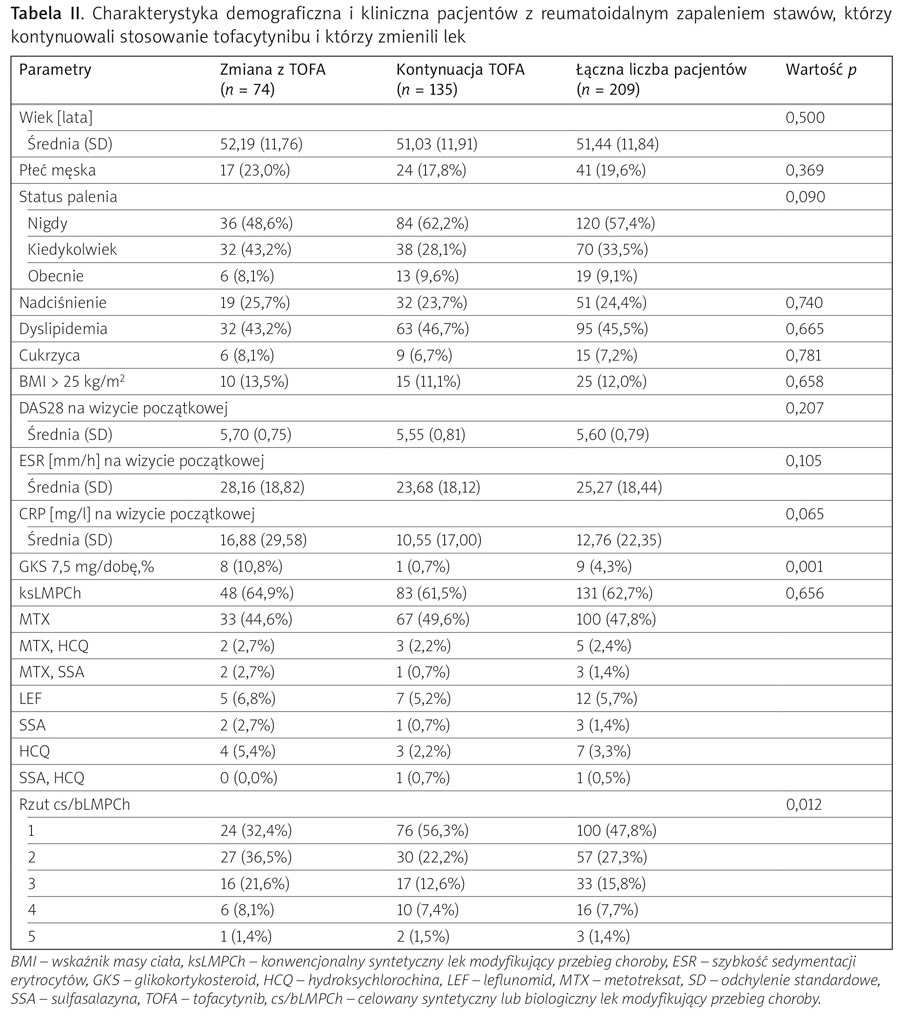
Najczęstszymi tradycyjnymi czynnikami ryzyka CV były: dyslipidemia (n = 95; 45,5%), nadciśnienie tętnicze (n = 51; 24,4%), BMI powyżej 25 kg/m2 (n = 25; 12%) i cukrzyca (n = 15; 7,2%). Tylko u 30 pacjentów (14,4%) w momencie rozpoczęcia leczenia TOFA nie występował żaden tradycyjny czynnik ryzyka CV.
Na podstawie prostej sumy czynników ryzyka pacjentów z RZS podzielono na charakteryzujących się niskim i wysokim ryzykiem CV, stosując 3-punktową granicę: 85 (40,7%) pacjentów z wysokim i 124 (59,3%) pacjentów z niskim ryzykiem. Tylko 9 (4,3%) pacjentów otrzymywało GKS w dawce >7,5 mg/dobę. Dziewięćdziesiąt osiem (46,9%) osób spełniło symulowane kryteria badania ORAL Surveillance, tj. wieku powyżej 50 lat i co najmniej 1 innego czynnika ryzyka CV. Rozkład ryzyka CV (na podstawie surowej liczby czynników ryzyka) przedstawiono na rycinie 1.

Większość pacjentów stosowała kombinację TOFA i konwencjonalnego syntetycznego LMPCh (n = 131; 62,7%) i byli to pacjenci otrzymujący innowacyjne leczenie pierwszego rzutu (n = 100; 47,8%; leczenie innowacyjne zdefiniowano jako zastosowanie jakiegokolwiek biologicznego LMPCh lub csLMPCh u nieleczonego wcześniej pacjenta). Rzadziej były to osoby otrzymujące leczenie drugiego (n = 57; 27,3%) i trzeciego rzutu (n = 33; 15,8%), a tylko 16 (7,7%) osób otrzymywało leczenie czwartego i 3 (1,4%) osoby piątego rzutu.
Mediana czasu obserwacji (IQR) w całej próbie wyniosła 16,9 (5,93–31,7) miesiąca.
W tej kohorcie RZS wskaźnik kontynuacji leczenia TOFA był wysoki. Po 6, 12 i 24 miesiącach medianę przeżycia (95% CI) oszacowano na, odpowiednio, 89,3% (85%, 93,9%), 82,4% (76,9%, 88,3%) i 60,4% (53,1%, 68,6%) (ryc. 2). Porównano charakterystykę kliniczną w zależności od statusu kontynuacji leczenia (tab. II).

Następnie zbadano kontynuację leczenia TOFA w zależności od częstości występowania ZN wymagających zmiany leku wśród użytkowników, u których wystąpiła odpowiedź na leczenie. Szacunkowa mediana (95% CI) kontynuacji stosowania leku po 6, 12 i 24 miesiącach wyniosła, odpowiednio, 92,8% (88,8%, 97%), 90,6% (86%, 95,4%) i 86,7% (81,1%, 92,8%) (ryc. 3).
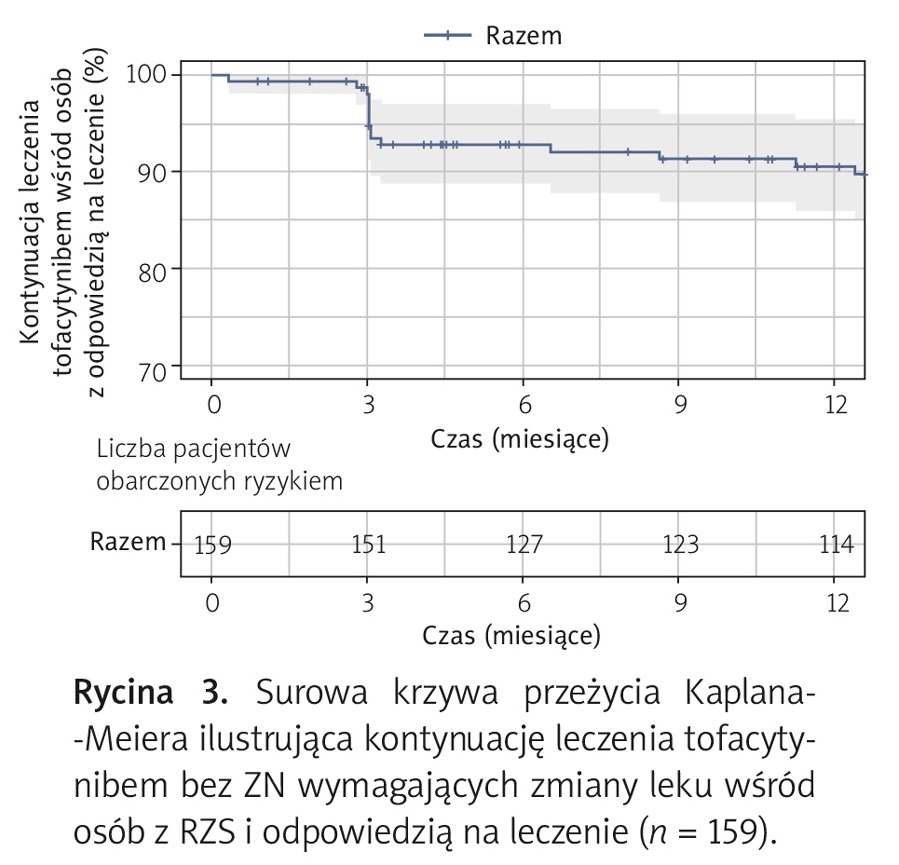
Przyczynami przerwania stosowania TOFA w całym okresie obserwacji u pacjentów z RZS były nieskuteczność (n = 50; 23,9%), ZN (n = 21; 10%) i inne, do których zaliczały się czynniki medyczne (remisja) i niemedyczne (np. decyzja pacjenta) (n = 3; 1,4%).
Po 6 miesiącach odnotowano 126 (60,3%) przypadków bez ZN. Jeden typ ZN zaobserwowano u 39 (17,7%) pacjentów, natomiast co najmniej dwa ZN zgłoszono u 46 (22,1%) osób. W ciągu pierwszych 6 miesięcy najczęstsze były zaburzenia lipidowe (34; 16,3%), zdarzenia infekcyjne (30; 14,4%) i zmiany w morfologii krwi (29; 13,9%). Ze względu na ramy czasowe zdarzenia wielokrotne traktowano jako jedno zdarzenie na pacjenta.
Pacjenci byli obserwowani aż do ostatniej dostępnej wizyty. Zgłoszono trzy przypadki zgonu: 2 pacjentów miało ciężkie zapalenie płuc wywołane wirusem COVID-19 (u 1 z nich było ono powikłane ŻChZZ), a stan kolejnego pacjenta pogorszył się w wyniku niewydolności oddechowej ze współistniejącą śródmiąższową chorobą płuc. Dodatkowo wystąpiły inne poważne ZN: 1 zakażenie COVID-19 niezakończone zgonem ze współistniejącą ŻChZZ, 1 ciężkie zapalenie płuc i 1 zapalenie uchyłka jelita z perforacją; szczególnie interesujące ZN zgłoszono w 3 przypadkach: w 1 nowotwór (rak piersi), w 2 ŻChZZ (wymienione powyżej).
Biorąc pod uwagę całkowitą sumę co najmniej 348 osobolat obserwacji pacjentów z RZS, odpowiadający współczynnik częstości występowania jakichkolwiek ZN wymagających zmiany leczenia wyniósł 60,34 (95% CI: 37,35–92,24) na 1000 osobolat obserwacji. Ze względu na wyjątkowo niski współczynnik zdarzeń nie dokonano podziału na konkretną przyczynę.
Ponadto zbadano, czy obciążenie CV wpływa na ogólny wskaźnik kontynuacji leczenia. W jednowymiarowym modelu PH Coxa współczynnik ryzyka kontynuacji stosowania TOFA wśród pacjentów z niskim ryzykiem CV wyniósł 1,62 (95% CI: 1,13–2,32; p = 0,008). Nie zaobserwowano związku pomiędzy statusem ryzyka CV a częstością występowania ZN (wymagających zmiany leku) wśród osób odpowiadających na leczenie z odpowiadającym HR wynoszącym 1,41 (95% CI: 0,57–3,52; p = 0,457). Dla nieskuteczności HR wyniósł 0,61 (95% CI: 0,35–1,06; p = 0,081) w podgrupie osób, u których nie wystąpiły ZN.
Uwzględniono także prosty model regresji logistycznej, obserwując mniejsze ryzyko nieskuteczności związane z niskim ryzykiem CV (OR 0,51, 95% CI: 0,27–0,95; p = 0,034) w całej kohorcie. Niskie ryzyko CV powiązano z przewidywanym prawdopodobieństwem wynoszącym 0,19 (95% CI: 0,13–0,26) w porównaniu z 0,32 (95% CI: 0,23–0,42) w grupie wysokiego ryzyka CV. Zilustrowano trendy czasowe różnych parametrów aktywności choroby i porównano je według statusu skuteczności (ryc. 4).

Dyskusja
Głównym wnioskiem niniejszego raportu jest to, że wskaźnik kontynuacji leczenia TOFA był wysoki w wieloośrodkowej kohorcie pacjentów z RZS rekrutowanych w różnych ośrodkach trzeciego stopnia referencyjności w całej Polsce. Główną przyczyną przerwania terapii przez pacjentów była nieskuteczność leczenia. Zaobserwowano również stosunkowo niski odsetek jakichkolwiek ZN we wczesnym, 6-miesięcznym okresie leczenia. Obserwacja aż do ostatniej dostępnej wizyty zapewniła dłuższy okres, w którym zarejestrowano tylko kilka ZN wymagających zmiany leku, co potwierdza aktualne parametry bezpieczeństwa dla TOFA. Ponadto obecność wielu tradycyjnych czynników ryzyka CV była związana z mniejszym wskaźnikiem kontynuacji leczenia TOFA i nieskutecznością.
Zaletą tego badania jest rzeczywisty charakter obserwacji, co wyklucza wprowadzenie niektórych źródeł błędów występujących w dokładnie kontrolowanych badaniach klinicznych i pozwala na bardziej etyczne postępowanie. Jest to jednocześnie pierwszy polski raport na ten temat. W raporcie tym uwzględniono wiele osób, które prawdopodobnie zostałyby wykluczone z badań (wcześniejsza choroba nowotworowa, sarkoidoza, twardzina skóry) lub nawet terapii (w przypadku części osób stosujących leki pierwszego rzutu TOFA nie byłby przepisywany zgodnie z zasadami FDA). Nie zaobserwowano żadnych trendów, które wskazywałyby na podwyższone ryzyko u tych osób.
W pewnym stopniu wskaźnik kontynuacji leczenia TOFA może być wyższy niż w innych badaniach, ale niższy w porównaniu z innymi kohortami europejskimi (86,5% w 12. miesiącu i 78,8% w 24. miesiącu w badaniu włoskim) [12].
Chociaż projekt badania wyklucza ocenę związków przyczynowo-skutkowych, dane te są ważne i należy dodać je do obecnego stanu oceny bezpieczeństwa TOFA. Należy zauważyć, że dzięki znajomości potencjalnego ryzyka związanego ze stosowaniem TOFA pacjenci mogą być częściej kontrolowani i intensywniej leczeni. Wykazano, że nie wszystkie czynniki ryzyka są jednakowe w kontekście stosowania TOFA, a najważniejszy wydaje się wywiad dotyczący choroby CV o podłożu miażdżycowym [13]. W kohorcie RZS, po wyłączeniu przypadków rozpoznanej choroby CV, wyższe ryzyko CV nadal miało negatywny wpływ na wskaźnik kontynuacji i skuteczność leczenia.
Odpowiedni styl życia i modyfikacja leczenia mogą zmniejszyć dodatkowe ryzyko związane z modyfikowalnymi czynnikami ryzyka CV [14]. Dotąd nie jest jasne, czy takie interwencje, jak leczenie statynami i konsekwentne osiąganie celów terapii nadciśnieniowej, mogą zmniejszyć nadmierne ryzyko CV związane z TOFA. Niestety, autorzy nie mogli wiarygodnie oszacować częstości występowania ZN o szczególnym znaczeniu ze względu na zbyt małą liczbę i stosunkowo niedużą wielkość próby. Główną przyczyną odstawienia była nieskuteczność, co jest również zgodne z wcześniejszymi doniesieniami [12].
Badanie ORAL Surveillance wykazało, że stosowanie TOFA może zwiększać ryzyko CV [3]. Podobne wnioski można wyciągnąć na podstawie kohorty STAR-RA, w której próbowano naśladować kryteria włączenia do badania ORAL. W badaniu STAR-RA natomiast częstość występowania zdarzeń CV była podobna jak w grupie TNFi [15].
We francuskich i duńskich kohortach chorych na RZS zaobserwowano, że ryzyko MACE i ŻChZZ w przypadku stosowania JAKi oraz bLMPCh nie różni się istotnie [16, 17]. Co zaskakujące, w niektórych doniesieniach ryzyko MACE wśród leczonych JAKi było nawet istotnie niższe niż w grupie leczonej TNFi [18, 19]. W niemieckim badaniu obserwacja ta dotyczyła nawet kohorty o wysokim ryzyku CV [20]. Z włoskich obserwacji w praktyce klinicznej wynika, że żadne zdarzenie CV nie spowodowało przerwania stosowania TOFA [12], ale pacjenci leczeni JAKi z wysokim ryzykiem CV byli narażeni na większe ryzyko wystąpienia ZN [21].
Porównując duże badania z randomizacją przeprowadzone dla TOFA w RZS, ZZSK, ŁZS i łuszczycy skóry, można zauważyć, że wyniki są stosunkowo spójne: częstość występowania poważnych ZN nie jest większa niż w grupie placebo [22], nie ma sytuacji uznanych za przypadki specjalnego zainteresowania ani ciężkich ZN [23–25].
Ogólnie można się spodziewać wyższego ryzyka wystąpienia MACE i ŻChZZ u osób stosujących TOFA w przypadku schematów z podaniem dużych dawek oraz u pacjentów ze zwiększonym wyjściowym ryzykiem CV. Choć badanie ORAL Surveillance nie wykazało równoważności TOFA w porównaniu z TNFi, nie jest ono jednoznaczne w odniesieniu do kardiotoksyczności, szczególnie w porównaniu z lekami o korzystnych profilach CV [26, 27]. Zapalenie odgrywa kluczową rolę w zarządzaniu ryzykiem CV [27], a u niektórych pacjentów złagodzenie stanu zapalnego można skuteczniej osiągnąć poprzez hamowanie osi sygnalizacyjnych związanych z TNF, podczas gdy u innych szlak JAK/STAT może być optymalnym celem terapii [28].
Ograniczenia badania
Badanie ma kilka ograniczeń. Istnieje możliwość błędu w selekcji: pacjenci z wysokim ryzykiem CV mogli mieć przepisywane leki inne niż JAKi.
Oprócz nieodłącznego błędu związanego z retrospektywnym charakterem i potencjalnymi brakami informacji w elektronicznej dokumentacji medycznej przeprowadzono łączenie danych i ręczny przegląd dokumentacji w celu uzupełnienia i zwiększenia wiarygodności zbioru danych. Co więcej, może występować błąd w przypisywaniu i przypominaniu danych, ponieważ ZN inne niż wyniki badań laboratoryjnych były w większości zgłaszane przez pacjentów.
Wszyscy pacjenci byli leczeni w ramach programu innowacyjnej terapii Narodowego Funduszu Zdrowia (NFZ), w którym po odstawieniu TOFA (jak również innych leków b/csLMPCh) ich ponowne wprowadzenie nie było możliwe. To ograniczenie mogło mieć wpływ na zgłaszanie ZN wymagających zmiany leku, powodując wahania w całym procesie decyzyjnym między reumatologami a pacjentami.
Nie można było także ocenić innych, współistniejących czynników ryzyka CV, takich jak skumulowana dawka GKS, indywidualny styl życia czy sprawność fizyczna.
Wnioski
W wieloośrodkowym, retrospektywnym badaniu kohortowym oceniano różne parametry skuteczności i bezpieczeństwa stosowania TOFA u pacjentów z RZS. Do mocnych stron tego raportu należą szczegółowe informacje z kraju Europy Środkowo-Wschodniej o niskim i średnim statusie dochodowym oraz wysoka wiarygodność danych dzięki ręcznemu przeglądowi dokumentacji medycznej i powiązaniu danych z dokumentacją z opieki ambulatoryjnej.
Wyniki tego badania wskazują na wysoki wskaźnik średnioterminowej kontynuacji stosowania leku i korzystny profil bezpieczeństwa (przy bardzo małej liczbie poważnych ZN), nawet pomimo zwiększonego ryzyka CV odnotowanego w tej kohorcie.
Karolina Palej, Kornelia Chmurzyńska i Krzysztof Batko nie zgłaszają konfliktu interesów.
Anna Felis-Giemza ma umowy na wystąpienia z firmami Pfizer, Abbvie, Biogen, Eli Lilly, Janssen, Novartis, Roche, Sandoz i UCB.
Zbigniew Guzera ma umowy na wystąpienia, umowy na badania kliniczne lub konsultuje dla firm Abbvie, Eli Lilly, Janssen, Merck Sharp & Dohme, Novartis, Pfizer, Roche i UCB.
Mateusz Moskal otrzymał granty od firm AbbVie, Medac, Novartis, Pfizer, Roche, Sandoz, UCB.
Marcin Stajszczyk ma umowy na wystąpienia, badania kliniczne lub konsultuje dla firm Abbvie, Amgen, Astra Zeneca, Biogen, Boehringer Ingelheim, Eli Lilly, Janssen, Merck Sharp & Dohme, Novartis, Pfizer, Roche, Sandoz, Swedish Orphan Biovitrum i UCB.
Piotr Wiland był prelegentem (otrzymał honoraria) dla firm Abbvie, Astra Zeneca, Eli Lilly, Medac, MSD, Novartis, Sandoz oraz był doradcą naukowym (otrzymał honoraria) firm Pierre Fabre i Pfizer oraz pełnił funkcję badacza w badaniach klinicznych dla: Biothera, BMS, Easthorn, Eli Lilly, Janssen, Novartis, Parexel i UCB.
Bogdan Batko ma umowy na wystąpienia, umowy na badania kliniczne i/lub konsultuje dla firm Abbvie, Amgen, Biogen, Bristol-Myers Squibb, Boehringer Ingelheim, Eli Lilly, Janssen, Merck Sharp & Dohme, Novartis, Pfizer, Roche, Sandoz i UCB.
Piśmiennictwo
1. Benucci M, Bernardini P, Coccia C i wsp. JAK inhibitors and autoimmune rheumatic diseases. Autoimmun Rev 2023; 22: 103276, DOI: 10.1016/j.autrev.2023.103276.
2. ChPL XELJANZ/XELJANZ XR/XELJANZ roztwór doustny. Wersja: grudzień 2021 r. Agencja ds. Żywności i Leków. Dostępne na: https://www.accessdata.fda.gov/drugsatfda_docs/label/2021/ 203214s028,208246s013,213082s003lbl.pdf (Dostęp: 24.07.2023).
3. Ytterberg SR, Bhatt DL, Mikuls TR i wsp. Cardiovascular and Cancer Risk with Tofacitinib in Rheumatoid Arthritis. N Engl J Med 2022; 386: 316–326, DOI: 10.1056/NEJMoa2109927.
4. Assessment report EMA/631064/2019. 31 October 2019. European Medicines Agency. Dostępne na: https://www.ema.europa.eu/documents/referral/xeljanz-h-20-1485-c-4214-0017-assessment-report-article-20_en.pdf (Dostęp: 19.07.2023).
5. FDA approves Boxed Warning about increased risk of blood clots and death with higher dose of arthritis and ulcerative colitis medicine tofacitinib (Xeljanz, Xeljanz XR). Safety announcement 7-26-2019. Food and Drug Administration. Dostępne na: https://www.fda.gov/drugs/drug-safety-and-availability/fda-approves-boxed-warning-about-increased-risk-blood-clots-and-death-higher-dose-arthritis-nad (Dostęp: 26.07.2023).
6. FDA requires warnings about increased risk of serious heart-related events, cancer, blood clots, and death for JAK inhibitors that treat certain chronic inflammatory conditions. FDA Drug Safety Communication 9-01-2021. Food and Drug Administration. Dostępne na: https://www.fda.gov/media/151936/download? attachment (Dostęp: 19.07.2023).
7. Assessment report EMA/586384/2022. 12 January 2023. European Medicines Agency. Dostępne na: https://www.ema.europa.eu/documents/referral/janus-kinase-inhibitors- jaki-article-20-pro-cedure-assessment-report_en.pdf (Dostęp: 18.07.2023).
8. Charles-Schoeman C, Buch MH, Dougados M i wsp. Risk of major adverse cardiovascular events with tofacitinib versus tumour necrosis factor inhibitors in patients with rheumatoid arthritis with or without a history of atherosclerotic cardiovascular disease: a post hoc analysis from ORAL Surveillance. Ann Rheum Dis 2023; 82: 119–129, DOI: 10.1136/ard-2022-222259.
9. Kristensen LE, Danese S, Yndestad A i wsp. Identification of two tofacitinib subpopulations with different relative risk versus TNF inhibitors: an analysis of the open label, randomised controlled study ORAL Surveillance. Ann Rheum Dis 2023; 82: 901–910, DOI: 10.1136/ard-2022-223715.
10. Wagan AA, Haider SN, Ahmed R i wsp. Modifiable cardiovascular risk factors in Rheumatoid Arthritis. Pak J Med Sci 2017; 33: 973–978, DOI: 10.12669/pjms.334.12798.
11. Stajszczyk M, Swierkowska G, Smolik K i wsp. The perspective of Polish patients with rheumatoid arthritis – treatment expectations, patient-reported outcomes, and digital literacy (the SENSE study). Reumatologia 2023; 61: 331–338, DOI: 10.5114/reum/171625.
12. Paroli M, Becciolini A, Bravi E i wsp. Long-Term Retention Rate of Tofacitinib in Rheumatoid Arthritis: An Italian Multicenter Retrospective Cohort Study. Medicina (Kaunas) 2023; 59: 1480, DOI: 10.3390/medicina59081480.
13. Dougados M, Charles-Schoeman C, Szekanecz Z i wsp. Impact of cardiovascular risk enrichment on incidence of major adverse cardiovascular events in the tofacitinib rheumatoid arthritis clinical programme. Ann Rheum Dis 2023; 82: 575–577, DOI: 10.1136/ard-2022-223406.
14. Corrao S. Crucial safety issues on Janus kinase inhibitors in rheumatoid arthritis might be associated with the lack of LDL-cholesterol management: a reasoned literature analysis. Intern Emerg Med 2023; 18: 2157–2161, DOI: 10.1007/s11739-023-03426-1.
15. Khosrow-Khavar F, Kim SC, Lee H i wsp. Tofacitinib and risk of cardiovascular outcomes: results from the Safety of TofAcitinib in Routine care patients with Rheumatoid Arthritis (STAR-RA) study. Ann Rheum Dis 2022; 81: 798–804, DOI: 10.1136/annrheumdis-2021-221915.
16. Hoisnard L, Pina Vegas L, Dray-Spira R i wsp. Risk of major adverse cardiovascular and venous thromboembolism events in patients with rheumatoid arthritis exposed to JAK inhibitors versus adalimumab: a nationwide cohort study. Ann Rheum Dis 2023; 82: 182–188, DOI: 10.1136/ard-2022-222824.
17. Popa CD, Opdam MAA, den Broeder N i wsp. Therapy with JAK inhibitors or bDMARDs and the risk of cardiovascular events in the Dutch rheumatoid arthritis population. Rheumatology (Oxford) 2023; kead531, DOI: 10.1093/rheumatology/kead531 [Online ahead of print].
18. Min HK, Kim H, Jeong HJ i wsp. Risk of cancer, cardiovascular disease, thromboembolism, and mortality in patients with rheumatoid arthritis receiving Janus kinase inhibitors: a real-world retrospective observational study using Korean health insurance data. Epidemiol Health 2023; 45: e2023045, DOI: 10.4178/epih.e2023045.
19. Frisell T, Bower H, Morin M i wsp. Safety of biological and targeted synthetic disease-modifying antirheumatic drugs for rheumatoid arthritis as used in clinical practice: results from the ARTIS programme. Ann Rheum Dis 2023; 82: 601–610, DOI: 10.1136/ard-2022-223762.
20. Meissner Y, Schafer M, Albrecht K i wsp. Risk of major adverse cardiovascular events in patients with rheumatoid arthritis treated with conventional synthetic, biologic and targeted synthetic disease-modifying antirheumatic drugs: observational data from the German RABBIT register. RMD Open 2023; 9: e003489, DOI: 10.1136/rmdopen-2023-003489.
21. Lanzillotta M, Boffini N, Barone E i wsp. Safety of Janus Kinase Inhibitors: A Real-World Multicenter Retrospective Cohort Study. J Rheumatol 2023; jrheum.2023-0145, DOI: 10.3899/ jrheum.2023-0145 [online ahead of print].
22. Kremer J, Li ZG, Hall S i wsp. Tofacitinib in combination with nonbiologic disease-modifying antirheumatic drugs in patients with active rheumatoid arthritis: a randomized trial. Ann Intern Med 2013; 159: 253–261, DOI: 10.7326/00034819-159-4-201308200-00006.
23. Leng X, Lin W, Liu S i wsp. Efficacy and safety of tofacitinib in Chinese patients with active psoriatic arthritis: a phase 3, randomised, double-blind, placebo-controlled study. RMD Open 2023; 9: e002559, DOI: 10.1136/rmdopen-2022-002559.
24. Deodhar A, Sliwinska-Stanczyk P, Xu H i wsp. Tofacitinib for the treatment of ankylosing spondylitis: a phase III, randomised, double-blind, placebo-controlled study. Ann Rheum Dis 2021; 80: 1004–1013, DOI: 10.1136/annrheumdis-2020-219601.
25. Asahina A, Etoh T, Igarashi A i wsp. Oral tofacitinib efficacy, safety and tolerability in Japanese patients with moderate to severe plaque psoriasis and psoriatic arthritis: A randomized, double-blind, phase 3 study. J Dermatol 2016; 43: 869–880, DOI: 10.1111/1346-8138.13258.
26. Solomon DH, Curtis JR, Saag KG i wsp. Cardiovascular risk in rheumatoid arthritis: comparing TNF-α blockade with nonbiologic DMARDs. Am J Med 2013; 126: 730.e9–730.e17, DOI: 10.1016/j.amjmed.2013.02.016.
27. Roubille C, Richer V, Starnino T i wsp. The effects of tumour necrosis factor inhibitors, methotrexate, non-steroidal antiinflammatory drugs and corticosteroids on cardiovascular events in rheumatoid arthritis, psoriasis and psoriatic arthritis: a systematic review and meta-analysis. Ann Rheum Dis 2015; 74: 480–489, DOI: 10.1136/annrheumdis-2014-206624.
28. Weber BN, Giles JT, Liao KP. Shared inflammatory pathways of rheumatoid arthritis and atherosclerotic cardiovascular disease. Nat Rev Rheumatol 2023; 19: 417–428, DOI: 10.1038/ s41584-023-00969-7.

